Aromatiklik nedir, şartları nelerdir, nasıl anlaşılır? Aromatik hidrokarbonların özellikleri, benzenin yapısı hakkında bilgi.
Aromatiklik ve Benzen
Sadece C ve H içeren bileşiklere hidrokarbonlar denir. Hidrokarbonlar,
1. Alifatik hidrokarbonlar (Alkan, alken, alkin ve bunların halkalı yapıda olanları)
2. Aromatik hidrokarbonlar şeklinde iki grupta incelenir.
Aromatik hidrokarbonlar doymamış yapıya sahip oldukları halde özel bir doymamışlık gösterdiklerinden ayrı bir sınıf olarak görülürler. Bütün aromatik bileşikler aromatik hidrokarbonların türevleridir. Organik kimyanın tümü
1. Alifatik bileşikler (Yağsıl bileşikler)
2. Aromatik bileşikler (Aramalı, güzel kokulu) olarak ikiye ayrılır.
Bir bileşiğin aromatik olması için,
1. Molekül halkalı olmalıdır.
2. Molekül tek düzlemli olmalıdır.
3. Halkada birer atlayarak çift bağlar ya da yükler bulunmalıdır.
4. Halkadaki pi(π) elektron sayısı (4n + 2) olmalıdır. Hückel kuralı olarak bilinen bu kurala göre, n = 0,1, 2, 3, 4, … gibi birer tamsayı olmalıdır.
O halde aromatik bileşikler 2, 6, 10, 14, …. pi(π) elektronuna sahiptirler.

Kekule, 1865 yılında benzen için günümüzde halen kullanılan ilk belirgin yapıyı önermiştir. Kekule, benzendeki karbon atomlarının halkada birbirlerini izleyen birli ve ikili bağlara bağlı olarak yer aldığı ve her bir karbon atomuna bir hidrojen atomunun bağlı olduğu bir yapı ileri sürmüştür.
Benzen’in formülü,
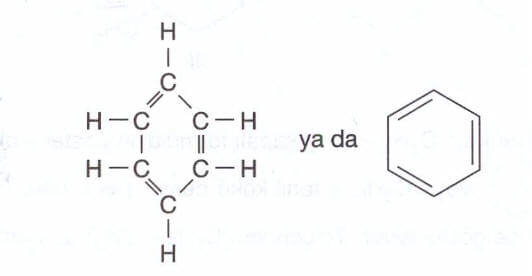
şeklindedir.
Ancak benzen yapısında birli ve ikili bağların hangi karbon atomları arasında olduğu bilinemez. Örneğin sadece bir tane 1,2 – dibrombenzen sentezlenebilmiştir.
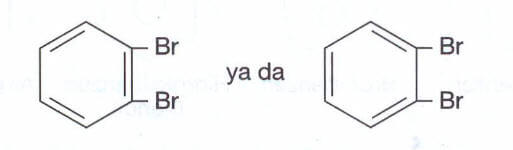
Bu iki bileşik aynıdır.
Çünkü bütün C – C ve C – H bağları her bakımdan (bağ uzunluğu, bağ enerjisi vb.) özdeştir. C – C bağ uzunluğu 1,39 A°, C – H bağ uzunluğu 1,09 A° dür. Bu nedenle benzen için iki farklı rezonans formülü yazılabilir.

I ve II rezonans yapıları arasına çift başlı bir ok (↔) konulur. Çift yönlü ok dengenin belirtilmesi için kullanılır. Benzen halkası doymamış olduğu halde kararlı bir yapıya sahiptir. (Katılma tepkimelerini güç, yer değiştirme tepkimelerini daha kolay verir.) Benzen molekülünde karbon atomları sp² hibritleşmesi yapmıştır. Buna göre, benzenin sigma bağları düzgün altıgen oluşturur, sp² hibritleşmesi yapan karbon atomlarından her biri üç adet sigma bağı oluşturur. Bu bağlardan ikisini komşu karbon atomlarıyla (sp² – sp²) üçüncüsünü ise hidrojen atomuyla (sp² – s) örtüşmesi gerçekleştirir. Benzen molekülündeki altı hidrojen atomu aynı düzlem üzerinde konumlanır ve bağ açıları 120° dir. C atomlarının oluşturduğu düzlemin altında ve üstünde simit biçiminde pi elektron bulutları yer alır.