Atom ağırlığı nedir? Bir atomun ağırlığı neyi ifade eder, nasıl ölçülür? Atom ağırlığı ve özellikleri hakkında bilgi.


Atom Ağırlığı
Bir atom ortadaki bir çekirdekle elektronlardan meydana gelmiştir. Elektronlar çok küçük olup çekirdeğin çevresinde bir yörünge üzerinde döner. Atomların birleşmesinde elektronlar en önemli rolü oynar. İki atom ancak dıştaki elektronları ortak kullanırsa ve bu elektronlar iki çekirdeğin çevresinde dönerse birleşebilir. Bu birleşmeden ortaya çıkan taneciğe molekül denir. Moleküller ikiden çok atomdan da meydana gelebilir. Sayfadaki şekil, karbon ve oksijen atomlarını gösteriyor, iki oksijen atomu dıştaki elektronlarını bir karbon atomuyla ortak kullanabilir. Sonuç, bir molekül karbondioksittir.
Atomlar birleşirken kendi özelliklerini tamamen kaybeder. Molekül kendini meydana getiren atomların hiç birine benzemez. Karbondioksidin oluşumunda iki oksijenle bir karbon atomu olaya girdiği için, bu molekülde ağırlıkça karbonun iki katı oksijen bulunacağı düşünülebilir. Ama bunda yanılırız. 44 gr. karbondioksidi ayrıştırırsak 32 gr. oksijen, 12 gr. karbon çıktığını görürüz. Çünkü bir karbon atomunun ağırlığı oksijenden daha azdır.
Bir atomun ağırlığı çekirdeğinde toplanmıştır. En hafif atom olan hidrojenin çekirdeğinde proton denilen bir tanecik bulunur. Öbür atomların çekirdeklerinde proton ve nötronlar, yani birden fazla tanecik bulunur. Bunların ağırlıkları birbirine çok yakın, hatta eşittir. Protonlar pozitif yüklü, nötronlarsa yüksüz (nötür) dür. Bir oksijen atomunun çekirdeğinde 8 proton ve 8 nötron, yani 16 tanecik vardır. Oksijen atomu hidrojen atomundan 16 kere daha ağırdır. Atomların ağırlıkları gram ölçüsünden çok küçük olduğu için yeni bir sistem kullanılır. Bir protonun ağırlığını birim alırsak (tanecik) 16 taneciği olan oksijen atomunun ağırlığı 16’dır. Karbonda 12 tanecik olduğundan karbonun atom ağırlığı 12’dir.
Atom Ağırlığının Ölçülmesi
Eşit sayıda karbon ve oksijen atomu almak için her 12 gr. karbona 16 gr. oksijen almamız gerekir. Karbon dioksit bileşiği karbonun iki katı oksijen istediği için 16×2 = 32 gr. oksijene ihtiyacımız vardır. Bu bileşikte 12 gr, da karbon olduğundan 32+12=44 gr. karbondioksit ortaya çıkar. Başka bir örnek olarak keskin kokulu ve boğucu bir gaz olan kükürtdioksidi alalım. Bu madde bir atom kükürt ve iki atom oksijenin birleşimidir. Kükürdün atom ağırlığı (32), oksijeninkinin (16) aynı değildir. Her 32 gr. kükürt için 16×2 = 32 gr. oksijene ihtiyacımız vardır. Bileşik 32 + 32 = 64 gr. ağırlığında kükürtdioksittir. Eğer fazla oksijen ya da kükürt kullanılırsa bunlar olaya girmez, artık kalır.
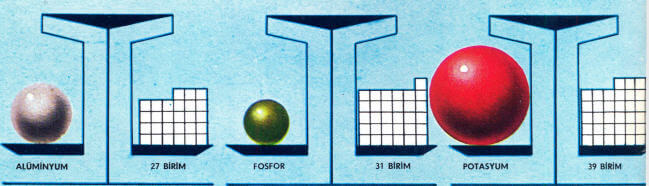
Resimlerde, atomların çekirdeğindeki tanecik sayıları terazinin sağ kolunda görülüyor. Bu sayı yuvarlak olarak atom ağırlığıdır. Şekilce en büyük atom en ağır olmayabilir. Atomun büyüklüğü elektronların dizilişine bağlıdır. Ama bu ağırlıklar her zaman tam sayılar değildir. Bunun nedeni, her saf elementin izotop adı verilen değişik atom şekilleri bulunmasıdır. Bunların, öbür atomlarla karşılaştırılınca ya da az, ya daha çok nötronları vardır. Onun için ağırlıkları farklıdır.