Berilyum elementinin özellikleri, atom numarası, bileşikleri, periyodik cetveldeki yeri, kullanım alanları, Berilyum elementi ile ilgili bilgi.
Berilyum Nedir? Berilyum Elementinin Özellikleri
Berilyum Grup 2 (IIA) elementidir. Bir metaldir ve yüksek bir erime noktasına sahiptir. Normal sıcaklıklarda, berilyum, hava oksidasyonu direnir. Berilyum bileşikleri çok zehirlidir. Cam çizilmeye kabiliyetini muhtemelen oksit ince bir tabaka oluşumu nedeniyle. Akuamarine ve zümrüt beril mineralinin değerli formlardır. [].
Berilyum be2 + şeklinde bir elektron kaybetmek eğilimindedir. Bu iyon çok küçüktür.
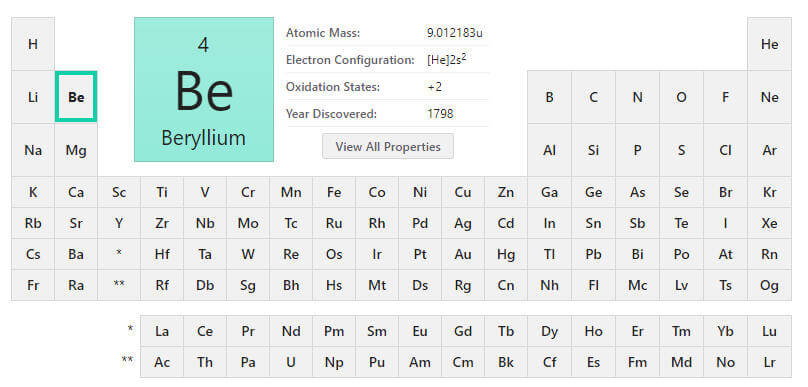
- Sembolü: Be
- Atom Numarası: 4
- Atom Ağırlığı: 9.012182(3) g/mol
- Elektron Sayısı: 4
- Elemet serisi: Alkalin
- Periyodik Tablodaki Yeri: 2A
- Maddenin Hali: Katı
- Görünümü: Beyaz-boz metalik
Fiziksel Özellikleri
Çelik grisi renkte parlak bir metaldir. Metallerin en hafiflerinden olup ısıyı iyi iletir. Magnetik değildir. Kırılgan ve hafif metallerin en sertlerinden biridir. Doğal berilyum kütle numarası 9 olan tek izotoptan oluşmuştur. Bunun dışında kütle numarası 6-8 ve 10-12 olan yapay radyoaktif izotopları yapılmıştır. Atom numarasının küçük olması nedeniyle X ışınlarına karşı yüksek geçirgenlik gösterir. Bu nedenle rönten tüplerinin pencerelerinin yapımında kullanılır.
Kimyasal Özellikleri
Kimyasal özellikler bakımından alüminyuma benzer. Periyodik çizelgenin II A grubunun birinci elementidir ve metallere özgü özelliklerin tümünü gösterir.
Elektron düzeni (He)2S2 ve yükseltgenme basamağı +2’dir. Adi sıcaklıkta havanın etkisine çok dayanıklıdır ve yüzeyi parlatılmış metal parlaklığını yıllarca korur. Yüksek sıcaklıklarda havada oksitlenmesi hızlanır, çok ince toz biçimindeki metal havadaki parlak bir alevle yanar. Yüzeyinde ince bir oksit filminin (tabakasının) oluşumu nedeniyle asitlere karşı dayanıklıdır. İnce dağılmış ya da amalgamlanmış metal seyreltik klorür, sülfat ve nitrat asitleriyle tepkimeye girdiği gibi alkalilerle de hidrojen çıkararak tepkimeye girer. Berilyum tuzlan sulu çözeltide hidrolizlenirler ve bu nedenle çözeltileri asit özelliği gösterir. Berilyum tuzlarının tatlı olması nedeniyle eskiden berilyuma glusinyum adı da verilmiştir. Berilyum ve tuzları zehirlidir. Düşük konsantrasyonlarda bile ölüme neden olurlar. Kronik zehirlenmelerde etkisi 3 ay – 15 yıl arası değişen bir süre sonra ortaya çıkar. İzin verilebilir sınır sekiz saatlik iş günü için 1m³ havada 2 mikrogram berilyum tozudur
Doğada Bulunuşu
Berilyum doğada yalnız bileşikleri biçiminde bulunur. Yerkabuğunda bulunma oranının % 0.001 olduğu sanılır. Berilyum içeren otuz dolayında mineral saptanmış olmakla birlikte bunların en Önemlileri aruaında beril krizoberi ve fenasit yer alır. Beril çeşitli metal oksitlerle renklenerek zümrüt, akuamarin gibi değerli taşları oluşturur. Berilyum elde edilmesinde ekonomik olan tek mineral berildir.
Kullanım Alanları:
Kullanımı bilgisayar parçaları ve jiroskop yapımı, uzay teknolojisi gibi birkaç özel alanla sınırlıdır. En önemli berilyum bileşiği berilyum oksittir (BeO). Ana madde olarak seramik eşya ve özel tip camlar yapmada, floresan tüplerinde, nükleer reaktörlerde kullanılır.
Berilyumun Elde Edilmesi:
Doğada bulunur, normal şartlarda laboratuvarda elde edilmez. Saf berilyum içeren erimiş BeCl2 ve NaCl elektrolizi ile elde edilebilir.Başka bir yöntem de, berilyum florürün 1300 derecedeki magnezyumla indirgenmesidir.
- BeF2 + Mg → MgF2 + Be
Alaşımları
Berilyum birçok alaşımın bileşimine girer ve alaşımlara sertlik verir. Berilyum bakır alaşımları yumuşak ve esnektirler ve 300°C’de ısıtıldıklarında yeniden sertleşirler. Dayanıklılık ve esneklilik gerektiren makine parçalarının yapımında kullanılırlar.
Berilyum-nikel alaşımları % 2 dolayında berilyum içerirler ve ısıtmayla büyük oranda esneklik ve sertlik kazandıklarından yüksek sıcaklıkta çalışan makine parçalarının yapımında kullanılırlar. Berilyum-demir alaşımları nikelli alaşımlara benzer özellikler gösterirler. Berilyum-alüminyum alaşımlarının yüksek dayanıklılıkları nedeniyle özellikle uçak, füze ve uzay araçlarının yapımında önemli bir yeri vardır.
Tarihçesi
Adı, içinde bulunduğu bir taş olan “beril” için Yunanca beryllos kelimesinden türemiştir (3BeO × Al2O3 × 6SiO2).
Berilyum, 1797 yılında Fransız kimyager ve eczacı Nicholas-Louis Vauquelin tarafından beril ve zümrüt tarafından keşfedildi. Eleman ilk olarak 1828’de Fransız kimyager Antoine-Alexandre-Brutus Bussy ve bağımsız olarak Alman kimyager Friedrich Wöhler tarafından ayrıldı. Berilyum tuzlarının tatlı bir tadı olduğu için, IUPAC 1949’da berilyum adını seçinceye kadar element, “tatlı” için Yunan glikozundan glusinyum olarak da biliniyordu.

63 yorum
çok işime yaradı teşkürrrrrrrrrrrrrrr
ÇOK AMA ÇOK İŞİME YARADIIIIIIIIIIIIIII
BU SİTELERİ YAPANI ALLAH KAZADAN BELADAN KORUSUSUN
tahsin hoca nerden bulur bu ödevleri anlamam allahım yaaaaaaaaaaaaaaaaa.:(
valla allah razı olsun cok lazım oldu !!!:…..
valla bu siteyi yapandan allah razı olsu çok işime yaradı fen ödevimde teşekkürler 🙂 🙂
valla billa ne diyim süper
süper
helal valla çok iyii 😀
gerçekten çok işime yaradı bu siteyi yapana tşk lerimi sunarım
Çok sağ olun! Harika yaptım ödevi. Hoca 😀 bizi çok uğraştırıyor ^_^
allah razı olsun çok işime yaradı
cok işime yaradı
çok işime yaradı thank you !
çok teşekkürederim bunda emeği geçen herkeze teşekkür ediyorum
saolun
ödevime çok yaradı
kimyadan 100 alacam bu sayfa sayesinde:)))))))))
işime yaradıda çok kısaydı yinede saolun elinize sağlık yapanların…
gerçekten iyi yaptım bu ödevi ama yararlı bir site sağolun elinize sağlık arkadaşlar…
allah razı olsun cok işime yaradı
muhteşem çok işime yaradı…:D
gerçekten çok güzel olmus işime cok yaradı sağalun
güzeldi sağolun :))
işime yaradı sağolun
çok iyi bir site güzel olmuş
Allah razı olsun çok işime yarayacak :))
cooook işime yaradı allah razı olsun. 🙂
ALLAH RAZI OLSUN HEPİNİZDEN ÇOK İŞE YARADI TEŞEKKÜRLER
çok teşekkürler çok işe yarası
tşk
işime çok yaradı
valla çok işime yaradı. Bu site olmasaydı 2 saatim aramakla geçerdi
süper
Bu siteyi yapandan ALLAH razı olsun çok işime yaradııııı….
birkaç yazıyla çok işime yaradı çok ama çok teşekkürler iki kelme yazı için de
proje ödevim için çok yararlı oldu size çok teşekkür ediyorum elinize sağlık
süperrrrrr 🙂 😉
ben şuan 4. sınıf öğrencisiyim[ilkokul) ama adımın elementi olması beni sevindirdi
çokkkkkkkkkkk güzel bir sitee
bencede
çok güzel bir site bayıldım
bence çok da güzel bir site bu site olmasaydı proje ödevimi 3 saat daha arardım yani elinize kolunuza sağlık çok beğendim bu siteyi <3 🙂
teşekkür ederim bu siteyi açanlara elinize kolunuza sağlık tekrardan da 🙂 😉 🙂 😉
çok iyi oldu bu site proje ödevim için çok teşekkürler 😀
çok iyi bi site 😀
çok iyi site sizde deneyin 😀
allah razı olsun çokkkkk güzel bi site
çokkk iyi oldu allah razı olsun 😀
coooook güzel teşekkür ederim 🙂
NBR
SÜPER BAYILDIM
Cok guzel hercekten keske biraz daha bileşik koysaydınız
Süper site çok güzel ama çok uzun
Bilgiler için çooook teşekkürler
Yorumunuzu Buraya Yazın çooook teşekkürler
çok güzel tüm ödevimi buradan yaptım çok güzel oldu teşekkür ederim hemde çooooooooooook
Mükemmel çok sağolun
very very thank you much
Cok saokun
UMARIM BİLGİLER DOĞRUDUR ÇÜNKÜ BULARLA LGS YE GİRCEMA
Sorumun cevabını buldum ama daha kısa olabilirdi
Yorumunuzu buraya özgürce yazabilirsiniz