Element ve bileşik nedir ve aralarındaki farklar nelerdir? Element ve bileşiğin ortak özellikleri ve farklı yönleri, fark tablosu.
Element ile Bileşik Arasındaki Fark
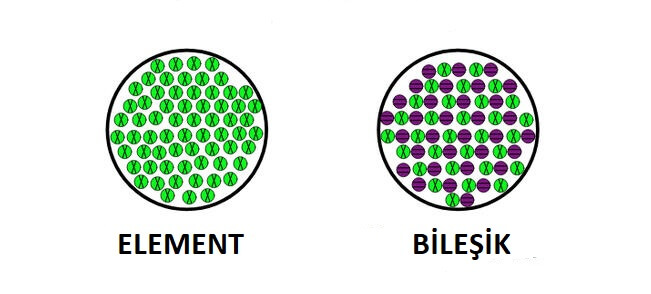
Elementler ve bileşikler doğada bulunan saf kimyasal maddelerdir. Bir element ile bir bileşik arasındaki fark, bir elementin aynı tipte bir atomdan yapılmış bir madde olması iken, bir bileşiğin belirli oranlarda farklı elemanlardan yapılmasıdır. Element örnekleri arasında demir, bakır, hidrojen ve oksijen bulunur. Bileşik örnekleri arasında su (H2O) ve tuz (Sodyum Klorür – NaCl) bulunur.
Elementler, Periyodik Tablodaki atom numaralarına göre listelenmiştir. Bilinen 117 element arasında, 94’ü doğal olarak karbon, oksijen, hidrojen vb. gibi meydana gelir. 22, radyoaktif değişiklikler geçiren yapay element vardır. Bunlara örnekler, Uranyum, Thorium, Bizmutdur. Elementler sabit oranlarda birleşerek bileşikleri meydana getirirler.
Farkların Tablosu
| Element | Bileşik |
| Bir element aynı tip atomdan yapılmış saf bir kimyasal maddedir. | Bir bileşik, kimyasal olarak sabit bir oranda bir araya getirilen farklı elementlerin atomlarını içerir. |
| Semboller kullanılarak bir element gösterilir. | Bir bileşik, bileşen elementlerinin sembollerini temsil eden kimyasal formülü ve bileşiğin bir molekülünde her bir elementin atom sayısını temsil eder. |
| Elementler yalnızca bir tür atom içerir. Her bir atom, aynı atom numarasına, yani çekirdeğinde aynı sayıda protona sahiptir. | Bileşenleri, kimyasal bağlar vasıtasıyla tanımlı bir şekilde düzenlenmiş sabit bir oranda farklı elementler içerir. Sadece bir tür molekül içerirler. Bileşiği oluşturan elemanlar kimyasal olarak birleştirilir. |
| Hidrojen (H), Oksijen (O), Sodyum (Na), Klor (Cl), Karbon (C), Demir (Fe), bakır ( Cu), gümüş (Ag), altın (Au) vb. elemet örnekleridir. | Su (H2O), Sodyum klorür (NaCl), Sodyum bikarbonat (NaHCO3) vs. bileşik örnekleridir. |
| Elementler, kimyasal reaksiyonlarla daha basit maddelere ayrıştırılamaz. | Bir bileşik, kimyasal yöntemler / reaksiyonlarla daha basit maddelere ayrılabilir. |
| Bilinen yaklaşık 117 eleman vardır. Metal, metal olmayan veya metaloid olarak sınıflandırılabilir | Neredeyse sınırsız sayıda kimyasal bileşik oluşturulabilir. Bileşikler, moleküler bileşikler, iyonik bileşikler, intermetalik bileşikler ve kompleksler olarak sınıflandırılır. |
Elementler
İsimleri, sembolleri, atom sayısı, erime noktası, kaynama noktası, yoğunluk ve iyonizasyon enerjileriyle ayırt edilir. Periyodik Tabloda, elementler atom numaralarına göre düzenlenir ve benzer kimyasal özelliklere göre gruplanır ve sembolleri ile tasvir edilir.
Atom numarası
Atom numarası Z harfi ile gösterilir ve element atomunun çekirdeğinde bulunan proton sayısıdır. Örneğin Karbonun çekirdeğinde 6 tane Proton vardır ve Karbon için, Z = 6’dır. Proton sayısı aynı zamanda elementin kimyasal özelliklerini belirleyen çekirdekte bulunan elektrik yükünün veya elektron sayısının göstergesidir.
Atomik Kütle
A harfi, elementin bir atomunun çekirdeğindeki toplam proton ve nötron sayısı olan elementin atomik kütlesini gösterir. Aynı elementlerin izotopları atomik kütlelerinde farklılık gösterir.
İzotoplar
Bir elementin izotopları, çekirdeklerinde aynı sayıda protona sahiptir ancak nötron sayısında farklılık gösterir. Doğal olarak oluşan elementlerin birden fazla kararlı izotopu vardır. Böylece izotoplar benzer kimyasal özelliklere (aynı sayıda protondan dolayı) fakat farklı nükleer özelliklerine (farklı nötron sayısına bağlı olarak) sahiptir. Örneğin Karbonun üç izotop, Karbon – 12, Karbon-13 ve Karbon – 14 vardır.
Allotroplar
Bir elementin atomları, kimyasal özelliklerinde farklılığa yol açan birden fazla şekilde birbirleriyle bağ oluşturabilirler. Örneğin Karbon, elmas ve altıgen şeklinde karbon formları grafiti oluşturmak için bir tetrahedronda bağlanır.
Bileşikler
Sabit bir oranda farklı elementlerden oluşur. Örneğin, 1 atom sodyum (Na), bir klor klorür (NaCI) bileşiği molekülü oluşturmak için 1 atomlu klor (Cl) ile birleşir. Bir bileşendeki elementler her zaman orijinal özelliklerini korumaz ve fiziksel yollarla ayrılmazlar. Elementlerin birleştirilmesi, değerliklerine göre kolaylaştırılmıştır. Çoğu bileşik katı olarak (yeterince düşük sıcaklık) mevcut olabilir ve ısı uygulamasıyla ayrışabilir. Bazen yabancı elementler, homojen olmayan bir yapı veren bileşiklerin kristal yapısının içine hapsedilir.