İdeal gaz yasası, ideal gaz sabiti ve ideal gazların davranış şekli nedir? Basınç ve ısı değişikliklerinde gazların davranışı ve ideal gaz denklemi.

İdeal Gaz Yasası
Eğer düdüklü tencere kullandıysanız, ideal gaz yasasından yararlanmışsınız demektir. Düdüklü tencereler nasıl çalışır? Bunlar pişirme sırasında buharın dışarı çıkmasını engelleyecek şekilde yalıtım uygulanmış tencerelerdir. Dışarıya hiç buhar kaçamadığı için su kaynadıkça içerideki buhar miktarı artar ve bu da basıncı yükseltir. Basınç daha fazla buharın oluşmasını önleyecek bir düzeye yükselir ve böylece yemek de suyun kaynama sıcaklığı olan 100 derece Celsius’tan daha çok ısınabilir. Bu durumda yemek daha çabuk pişer ve böylece lezzetinden bir şey kaybetmez.
İlk kez Fransız fizikçi Emile Clapeyron’un 19. yüzyılda sözünü ettiği ideal gaz yasası, bir gazın basınç, sıcaklık ve hacminin birbiriyle bağlantılı olduğunu söyler. Hacim küçüldüğünde ya da sıcaklık arttığında gazın basıncı yükselir. İçinde hava bulunan bir kutu düşünün. Eğer kutunun hacmini yarıya düşürürseniz basınç iki katına çıkar. Eğer kutuyu ısıtarak sıcaklığını iki katına çıkarırsanız, basınç yine iki katına çıkar.
İdeal gaz yasası PV = nRT şeklinde yazılır. Burada P basınç, V hacim, T sıcaklık, n gazın mol sayısı (1 mol’de Avogadro sayısı kadar, yani 6×10^23 tane atom bulunur) ve R gaz sabiti denen bir sayıdır.
Clapeyron ideal gaz yasasını türetirken daha önce bulunan iki yasayı birleştirmişti: biri Robert Boyle’un basınçla hacim arasındaki ilişki yasası, diğeri de Jacques Charles ve Joseph Louis Gay-Lussac’ın hacimle sıcaklık arasındaki ilişki yasası. Clapeyron bu üç niceliği birleştirirken bir mol gaz üzerinden düşünmüştü. Bir mol, 6×1023-yani 6 ve ardından 23 tane sıfır— tane atom ya da molekül” miktarı demektir ki bu sayıya Avogadro sayısı da denir. Bu kadar çok atomun müthiş yer kaplayacağını düşünebilirsiniz ama aslında bir kurşunkalemin içindeki grafitte de yaklaşık bu kadar atom vardır. Bir mol, 12 gram karbondaki karbon-12 atomlarının sayısı olarak tanımlanmıştır. Avogadro sayısının büyüklüğünü şöyle de düşünebilirsiniz: Avogadro sayısı kadar greyfurtunuz olsaydı, hacmi Dünya kadar olurdu.
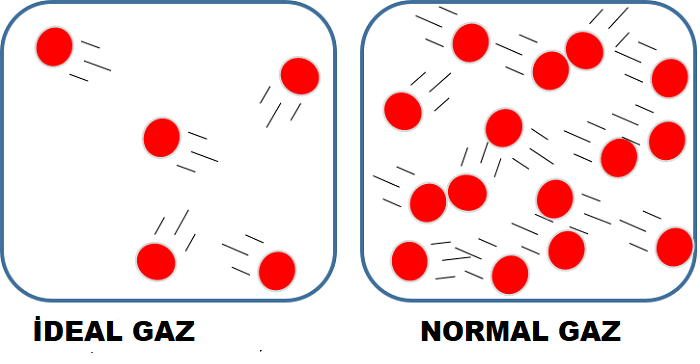
Peki ideal gaz nedir?
Basitçe söylersek, ideal gaz yasasına uyan gazdır. Buna uyar çünkü gazı oluşturan atomlar veya moleküller, aralarındaki mesafelere oranla çok küçük olduklarından, birbirlerine çarpmadan, rahatça hareket edebilirler. Bunun yanında parçacıkları birbirine yapışmaya zorlayacak -örneğin elektriksel yükler gibi- başka kuvvetler de yoktur.
Neon, argon ve ksenon gibi “soy gazlar”, (moleküllerden değil de) atomlardan oluşan ideal gazlar gibi davranırlar. Hidrojen, azot ve oksijen gibi simetrik, hatif moleküller de neredeyse birer ideal gaz gibi davranır. Ama bütan gibi daha ağır gaz molekülleri bu ideallikten uzaktır.
Gazların yoğunlukları çok düşük olur. Gazı oluşturan atomlar veya moleküller bir arada durmazlar ve ortamda serbestçe dolaşırlar. İdeal gazlarda atomlar, tıpkı bir duvar tenisi salonuna bırakılmış binlerce lastik top gibi birbirlerine ve oyun alanının duvarlarına çarpıp sekerler. Gazların sınırları olmasa da kapalı kapların içinde tutulabilirler. Kabın boyutlarını küçültmek gaz moleküllerini birbirlerine yaklaştırır ve gaz yasasına göre hem basıncı hem de sıcaklığı arttırır.
Gaz basıncı, atomlar veya moleküller havada dolaşırken kabın duvarlarına ve birbirlerine çarpmalarından kaynaklanır. Newton’ın üçüncü yasasına göre, seken parçacıklar duvarlara ters yönlü bir kuvvet uygular. Duvarlarla parçacıklar arasındaki çarpışmalar esnektir. Dolayısıyla parçacıklar hiçbir yapışma ya da enerji kaybı olmadan sekerler ama kaba momentumlarını aktarırlar ve bu da basınç şeklinde hissedilir. Momentum normalde kabı dışa doğru ittirecekken kabın sağlamlığı buna karşı koyar. Ayrıca çarpışmalardan dolayı her yöne doğru kuvvetler oluştuğundan bunlar toplamda birbirini götürür.

Sıcaklığı arttırmak parçacıkların hızını arttırır. Böylece duvarlara uygulanan kuvvetler Yüksek basınç büyür. Isı enerjisi moleküllere geçerek kinetik enerjilerini arttırır ve daha hızlı hareket etmelerine neden olur. Moleküller de duvarlara çarptıklarında artık daha büyük momentum aktardıklarından basınç yükselir.
Hacmi düşürmek gazın yoğunluğunu arttırır. Böylece atomlar veya moleküller duvarlara daha çok çarpar ve basınç yine artar. Sıcaklık da yükselir, çünkü enerji korunduğu için daha küçük bir alanda hareket eden moleküllerin hızı artar.
Bazı gazlar bu yasaya tam uymaz.
Büyük ya da karmaşık moleküllü gazların molekülleri arasında bazı ek kuvvetler ortaya çıkar ve molekülleri öbekler oluşturmaya meylettirir. Bu tür yapıştırıcı kuvvetler, molekülleri oluşturan atomların elektrik yüklerinden kaynaklanır ve genellikle (gaz çok sıkıştırıldığı ya da çok soğuk olduğu için) moleküllerin hareketi yavaşladığında ortaya çıkarlar. Protein ve yağ gibi çok yapışkan moleküller gaz haline geçmezler bile.

Basınç ve yükseklik Dağa tırmanırken üzerinizde daha az atmosfer olduğu için üzerinizdeki atmosfer basıncı da deniz düzeyine göre daha az olur. Dikkatinizi çektiyse bu durumda hava sıcaklığı da düşer. Yolcu uçaklarının uçtuğu yüksekliklerde hava sıcaklığı donma derecesinin çok altındadır. Bu da aslında ideal gaz yasasının güzel bir örneğidir.
Yüksek irtifada atmosfer basıncı düşük olduğu için, su deniz seviyesine oranla daha düşük sıcaklıklarda kaynamaya başlar. Yiyecekler iyi pişmediği için dağcılar bazen düdüklü tencere kullanır. Fransız fizikçi Denis Pa-pin’in 17. yüzyılın sonlarında düdüklü tencereyi icat ettiğini bilen Charles Darwin de 1835’de Andları dolaşırken yanında bir tane bulunmamasından yakınmıştır.
Beagle Yolculuğu günlüklerinde Darwin şöyle yazmıştı:
“Uyuduğumuz yerde atmosfer basıncı düşük olduğu için su alçak kesimlere oranla daha düşük bir sıcaklıkta kaynıyordu; yani Papin’in kazanındakinin tersi bir durum söz konusuydu. Dolayısıyla patatesler de kaynar suda saatlerce kalmalarına rağmen hâlâ taş gibi oluyordu. Tencere gece boyunca ateşte kaldı ve ertesi sabah yeniden kaynatıldı ama patatesler yine de pişmedi. Bunun nedeni üzerine tartışan iki yol arkadaşıma kulak misafiri olunca vardıkları kestirme sonucu öğrenmiş oldum: ‘Bu yeni tencere lanetli. Patatesleri pişirmek istemiyor.”
Vakum
Dağları da geçip atmosferin üstüne, yani uzaya çıkarsanız basınç neredeyse sıfıra düşer. Kusursuz bir vakum “ortamında hiç atom olmaz. Ancak Evren’in hiçbir verinde kusursuz vakum yoktur. Uzay boşluğunda bile santimetreküp başına birkaç hidrojen atomu bulunur. Eski Yunan düşünürleri Platon ve Aristoteles, “hiçbir şey” diye bir şey var olamayacağı için kusursuz vakumun da olamayacağına inanıyorlardı.
Günümüzde kuantum mekaniği, hiçbir şeyin bulunmadığı bir vakum düşüncesini bir kenara kaldırmıştır, çünkü kuantum kuramına göre boşluk dediğimiz şey sürekli yokluktan var olup yeniden yok olan sanal atom-altı parçacıklarla kaynar durur. Hatta kozmolojiye göre boşlukta Evren’in genişlemesini hızlandıran ve karanlık enerji adıyla bilinen negatif bir basınç olabilir. Anlaşılan, doğa gerçekten de boşluktan nefret ediyor.