Rutherford Atom Modeli nedir? Rutherford Atom Modelinin özellikleri nelerdir, açıklaması, şekilli anlatımı, özeti, hakkında bilgi.
Rutherford Atom Modeli
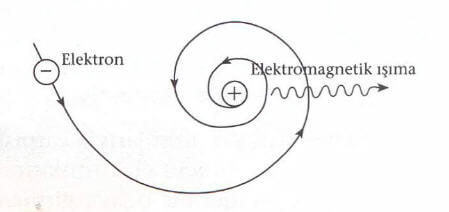
Rutherford radyoaktif maddelerden çıkan yüksek hızlı α tanecikleriyle bombardıman ettiği çok ince altın yapraklardan α taneciklerinin saçılmasını inceleyip yeni bir atom modeli geliştirdi, tik defa atomun çekirdekli yapıda oluşu fikri bu modelle ortaya atılmış olup α taneciklerinin altın levha üzerine gönderildiğinde keskin sapmaların oluşu bu fikri doğrulamıştır. Bu modele göre atom merkezde ortada pozitif yüklü ağır bir çekirdek ve bunun çevresinde dolanan elektronları ile birlikte güneş sistemine benzetildi. Burada gezegenlerin kütle çekimi ile güneş çevresinde dolandığı gibi elektronlar da çekirdek çevresinde elektriksel çekim kuvveti ile dolanırlar. Negatif yüklü elektronlar çekirdeğin pozitif yükünün etkisini karşılar ve atom nötr görünür.
Neden Kusurlu Bir Modeldir?
Rutherford atom modeli temelde doğru gibi görünüyorsa da elektronların davranışını incelemeye başladığımız zaman iki önemli sebepten dolayı kusurlu olduğu anlaşılmıştır.
1. Elektronların Coulomb çekim kuvveti ile pozitif yüklü çekirdek çevresinde dolanmaları sırasında ivmeli hareket yapması, elekromagnetik ışımanın yayılmasına sebep olur. Işıma yapan elektron da enerji kaybederek spiral yörünge üzerinde çekirdeğe yaklaşır ve atomik sistemin çökmesi ile sonuçlanır. Atom çöküp yok olmadığına göre bu model yetersiz kalmıştır.
2. Atomdan yayılan ışığın frekansı, elektronun çekirdek çevresinde saniyede yaptığı dönme sayısına bağlıdır. Elektron daha küçük yarıçaplı yörüngede dolanırsa frekansı daha büyük olacak, çapı gittikçe küçülen yörüngede dolanan elektronun yaydığı ışığın frekansı da gittikçe artacaktır.
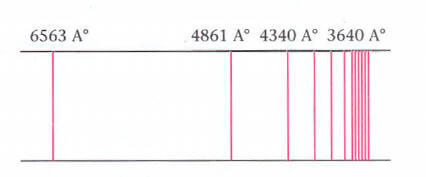
Bir ışık kaynağında çok sayıda atom vardır. Buna göre kaynak hemen hemen bütün frekanslarda ışık yayarak sürekli bir ışık spektrumu vermelidir. Oysa hidrojen gazının spektrumu incelendiğinde belli sayıda keskin çizgiler görülür ki bu da belli sayıda farklı dalga boylan veya frekansların var olduğunu, bu belli frekanslar ise ışımaların kesikli ve belli enerjilere sahip olduklarını böylece elektron yörüngelerinin çekirdekten belli uzaklıkta bulunabileceğini göstermektedir. Yani elektronun çekirdeğe sürekli yaklaşmadığını gösterir. O halde bir atomun iç enerjisi ancak dışarıya verilen veya dışarıdan alınan belli enerji miktarları kadar değişebilir.