Hidrokarbonlar nelerdir? Hidrokarbonların kimyasal yapısı, çeşitleri ve özellikleri nelerdir? Hidrokarbonlar hakkında bilgi.
Hidrokarbonların Özellikleri
Hidrokarbonlar yapısında sadece karbon ve hidrojen elementlerini içeren organik bileşiklerdir. Diğer bazı organik bileşiklerde C ve H nin yanında oksijen, azot atomları da bulunabilir.
Karbon, Oksijen, Azot ve Hidrojen Atomunun Bağ Yapma Özellikleri
Bahsedilen bu dört elementin elektron dağılımını yaparak yapabileceği bağ sayılarını inceleyelim.
Elementler dublet ya da oktede ulaşmak için elektron alır ya da verirler. Son katmanında 1 elektronu olan H elementi 1 elektron alarak dublete ulaşır. 1 elektron alması H nin 1 bağ yaptığı anlamına gelir.
Son katmanında 5 elektronu olan N elementi 3 elektron alarak oktede ulaşır. 3 eleKtron alması N nin 3 bağ yaptığı anlamına gelir.
Son katmanında 6 elektronu olan O elementi 2 elektron alarak oktede ulaşır. 2 elektron alması O nin 2 bağ yaptığı anlamına gelir.
Son katmanında 4 elektronu olan C elementi 4 elektron alarak oktede ulaşır. Karbon atomu 4 elektron aldığından dolayı kararlı bileşiklerinde 4 tane bağ yapar. Bu durum organik bileşiklerin sayısının çok fazla olmasını sağlar. Bu bağları diğer atomlarla ya da başka C atomu ile de yapabilir. Ayrıca C atomu diğer elementlerle tekli, ikili ve üçlü bağlar yapabilir.
Karbon atomu bu 4 bağını,
***Hep tek bağ olarak 4 ayrı atomla yapabilir.
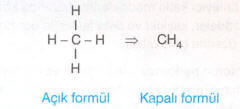
***Bir atoma 1 tane ikili bağla bağlanıp, diğer iki atoma tekli bağlarla bağlanarak 3 ayrı atoma bağlanabilir.

***Bir atoma 1 tane üçlü bağ ile bağlanıp, diğer bir atoma tekli bağla bağlanarak 2 ayrı atoma bağlanabilir.

Yukarıda da görüldüğü gibi organik bir bileşiğin formülü 3 farklı şekilde yazılabilmektedir. Biz bu konuda daha çok yarı açık formülleri ve kapalı formülleri kullanacağız.
Organik bileşikler sınıflandırdığında hidrokarbonlar ve fonksiyonlu grup içerenler olmak üzere temelde ikiye ayrılır.
Aşağıda bazı organik bileşikler verilmiştir. Bütün bileşiklerde C ve H oluşuna dikkat edilmelidir.
Günlük hayatta kullandığımız eşyaların, giyeceklerin, yiyeceklerin ve daha bir çok maddenin yapıtaşı organik maddedir.
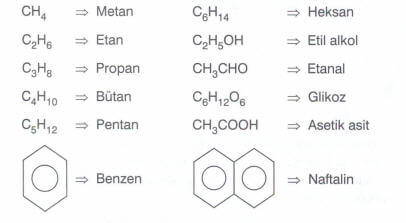
Organik maddelerin bu şekilde çok sayıda olmasının nedeni C atomunun çok sayıda çeşitlilikle birbirine bağlanabilme kabiliyeti ile ilgilidir.
ALKANLAR
DİĞER HİDROKARBONLAR
Karbon atomları arasında en az bir tane ikili bağ (C = C) içeren hidrokarbonlar alkenler ve en az bir tane üçlü bağ (C = C) içeren hidrokarbonlar alkinler olarak sınıflandırılır.
Alkenlerin en küçük üyesi 2 karbonlu olan ve alkinlerin en küçük üyesi 2 karbonlu olan
bileşikleridir.
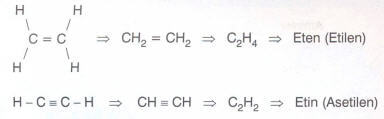
Bu bileşiklerden etilen polimer maddelerin üretiminde, asetilen ise oksijen kaynaklarında kullanılan maddelerdendir.
Alken ve alkinlerin bu en küçük iki üyesinin dışında küçükten büyüğe doğru çok fazla türde bileşikleri vardır.
AROMATİK HİDROKARBONLAR
Hidrokarbonların en önemli türlerinden birisi de aromatik halka içeren bileşiklerdir. Bu bileşiklerde halkadaki karbon atomları arasında bir tekli bir çiftli bağ olacak şekilde bir dizilim vardır. Aromatik hidrokarbonların en önemlisi benzen bileşiğidir. Kapalı formülü şeklindedir.
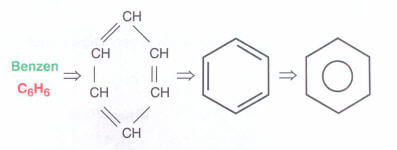
Benzen halkasına metil () grubu bağlanırsa toluen, amin (
) grubu bağlanırsa anilin oluşur. Halkada azot atomu bağlı ise pridin oluşur.
Hidrokarbonlar yandığında enerji açığa çıkar. Kontrollü yakma sonucunda bu ısıları kullanırız. Metanın yanma tepkimesi,
şeklindedir. Tepkimeden 16 g metan yandığında 886 kJ ısının çıkacağı anlaşılır.
Not Hidrokarbonlar,
***Yandıklarında ve
açığa çıkar.
***Apolar karakterli olduklarından suda çözünmezler.