Hidrojen elementinin özellikleri, atom numarası, bileşikleri, periyodik cetveldeki yeri, kullanım alanları, tarihçesi, Hidrojen elementi ile ilgili bilgi.
Hidrojen
Hidrojen en hafif elementtir. Evrende en bol bulunan elementtir ve ağırlığına göre, evrenin yaklaşık % 90’ınını oluşturur. Yaşam için su, su (H2O) için hidrojen kesinlikle gereklidir ve tüm organik bileşikler bulunur. Hidrojen hafif bir gazdır. Hidrojen gazı hafif hava balonları taşımacılığı için kullanılmıştı ancak yangın riskinin yüksek olması nedeniyle çok tehlikeli idi. Hidrojen, yanma sonrası atık ürün olarak sadece su oluşturduğundan dolayı, bir hidrojen ekonomisinin gelişme olasılığı mümkündür.
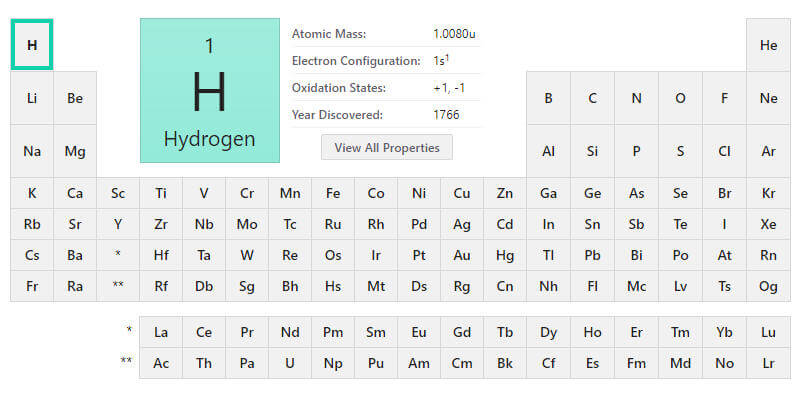
- Sembolü: H
- Atom Numarası: 1
- Atom Ağırlığı: 1.00794(7) g/mol
- Elektron Sayısı: 1
- Element serisi: Ametal
- Periyodik Tablodaki Yeri: 1A
- Maddenin Hali: Gaz
- Görünümü: Renksiz
Özellikleri
Hidrojen suda çok az çözünür ve iyi bir iletkendir. Difüzyon özelliği nedeniyle delikli ya da gözenekli çeperlerden kolayca geçer, be nedenle çelik koruyucularda saklanır. Alkali metal olmamasına karşın alkali metaller grubunda bulunur. En büyük özelliği indirgen oluşudur. Hava ya da oksijen içinde yanarsa suyu oluşturur.
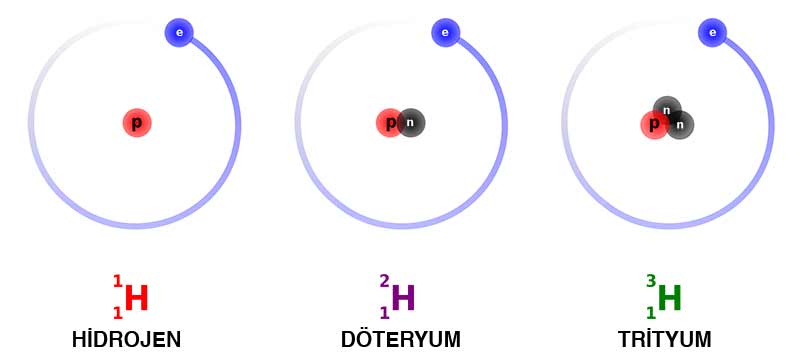
Döteryum:
D simgesiyle gösterilir. İlk olarak 1932’de Amerikalı kimyacı Harold C Urey tarafından gözlendi. Ağır suyun hazırlanmasında kullanılır. (D2O) Suyun elektroliziyle elde edilir. Doğal hidrojen içinde döteryum hidrojenin tersine nötronları soğurmadan yavaşlatma özelliği vardır. Özellikle atomların sayısının prdyum atomlarına oranı 1/6000 kadardır. Atom pillerinin doldurulmasında ağır su olarak kullanılır.
Hidrojenin Kullanım Alanları:
Hidrojen ticari olarak önemli bir elementtir. Bir işlemle amonyak () üretmek için büyük miktarlarda hidrojen havadan azot ile birleştirilir. Hidrojen ayrıca, fıstık yağı gibi katı ve sıvı yağlara hidrojenasyon adı verilen bir işlemle ilave edilir. Süper iletkenlerin çalışmasında sıvı hidrojen kullanılır ve sıvı oksijen ile birleştirildiğinde mükemmel bir roket yakıtı yapar.
Hidrojen diğer elementlerle birleşerek çok sayıda bileşik oluşturur. Yaygın olanlardan bazıları şunlardır: su (), amonyak (
), metan (
), sofra şekeri (
), hidrojen peroksit (
) ve hidroklorik asit (HCl).
Hidrojenin üç ortak izotopu vardır. Protium adı verilen en basit izotop sadece sıradan hidrojendir. İkincisi, döteryum adı verilen stabil bir izotop 1932’de keşfedildi. Üçüncü izotop, trityum, 1934’te keşfedildi.
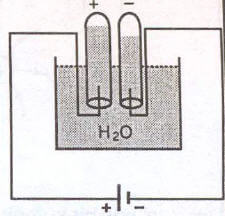
suyun elektrolizi
Hidrojenin Elde Edilmesi:
Endüstride hidrojen çoğunlukla suyun elektrolizinden, doğal gazdan ve petrolün damıtılması sırasında oluşan rafineri gazların nikel katalizör üzerinde su buharıyla birlikte 700-800 dereceye kadar ısıtılarak elde edilir. Elektroliz yöntemiyle hidrojenin eldesi özellikle elektriğin bol ve ucuz elde edildiği ülkelerde kullanılır. Su, baryumhidroksit ya da sodyumhidroksit ile iletken duruma getirilir ve elektrikle su ayrıştırılır. Ayrıca kok ile sudan da elde edilir. Sıcak kömürün üzerinden su buharı geçirilir. Ortaya çıkan su gazı ve buharıyla karıştırılarak katalizörlerden geçirilir. İçindeki karbonmonoksite dönüşür. Bu hidrojen ve kardondioksit suya tutulur, geriye kalan bileşim arındırılarak hidrojen elde edilir. Laboratuvarda, küçük miktarlarda hidrojen gazı kalsiyum hidrürün su ile reaksiyona girmesiyle yapılabilir.
- CaH2 + 2H2O → Ca (OH) 2 + 2H2
Bu üretilen hidrojen ile birlikte % 50 su elde edildiğinden oldukça verimlidir. Bir başka laboratuvar ölçekli deney Boyle’un deneyi olan seyreltik sülfürik asit ile demirin reaksiyonudur.
- Fe + H2SO4 → FeSO4 + H2
Diğer iki hidrojen üreten reaksiyon ise;
- CH4 + H2O (1100 ° C) → CO + 3H2
C (kok) + H2O (1000 ° C) → CO + H2

Tarihçesi ve Keşfi
Bilim adamları, element olarak tanınmadan önce yıllardır hidrojen üretiyorlardı. Yazılı kayıtlar, Robert Boyle’ın 1671 gibi kısa bir sürede demir ve asitlerle deney yaparken hidrojen gazı ürettiğini göstermektedir. Hidrojen ilk olarak 1766’da Henry Cavendish tarafından ayrı bir element olarak kabul edildi. Tek bir proton ve tek bir elektrondan oluşan hidrojen, evrendeki en basit ve en bol elementtir. Görünür evrenin% 90’ının hidrojenden oluştuğu tahmin edilmektedir.
Hidrojen, çoğu yıldızın enerji üretmek için ‘yaktığı’ ham yakıttır. Füzyon olarak bilinen aynı süreç, dünyada kullanım için olası bir güç kaynağı olarak incelenmektedir. Güneşin hidrojen arzının 5 milyar yıl daha sürmesi bekleniyor.
36 yorum
Çok güzel bi site emeği geçen herkese teşekkür hihihih 😀 😀 😀 😀 😀 😀 😀 😀 😀 😀
emeği gecen herkese teşekkür ederim.proje ödevini burdan yapıyorum =D
çokzel ben directionerimde 😀
çok güzel bir siyte
çok beğendin
i think its a very populer asite but wharts can i do sometimes
süper emegi geçenlere teşk 🙂 🙂 🙂 <3
bencede helyum.. anladınmı
çk güzel bence süper bişi herkese tşkrler
çok saolun 😀 😀 😛
Cok guzel bi site emegi gecen herkese tesekkurler bu arada anti beliberim
süper olmuş elinize sağlıık 😀
çok güzel
emeği geçenlere teşekkürler
sağol canım
neden sagol dedin
güzel hidrojen enerjisi ne onuda bir öğrensek
çok güzel .12.5.2014
çok güzel bir site
gercekten öyle<*
abi süper
bence çççççççççççooooooooooooookkkkkkkkkkkkk güzel
süpersiniz performanstan 100 aldım
HAZIRLAYAN HERKESE SONSUZ TEŞEKKÜRLER
SÜPERSİNİZ
harika en güzel açıklama bu sayfada
cok iyi geldi tesekkurler herkese
çok teşekkürler proje ödevim için gerekli olanları kullandım ama güzel olmuş
Çok teşekkürler çok yardımcı oldu gerçekten.
“ya da” diye yazılacak. Bilginize…
Düzeltilmiştir…
Çok teşekkür ederim proje ödevime çok katkı sağladı bütün bilgiler bu sayfada çok sağolun ?
Görüldüğü gibi 1100 santigrat derecede ki su buharına 1 m3 doğal geçirildiğinde 3 m3 Hidrojen gazı ile 1m3 CO gazı elde edilmektedir. Ekonomiklik ve kullanım alanının çeşitliliğine göre iyi bir durumdur. İsmail ÖZCAN
Ne’kadada gözel
çok tesekurler odevım için çok yardımcı oldu
çok harika bir sayfa teşekkürler
çoook güzel
işte en sevdiğim element
ı love you hidrojen