Asitlerin kuvvetli ve zayıf olduğu nasıl belli olur, aralarındaki fark nedir? Asitlerin kuvvetliliği, zayıf ve kuvvetli asit örnekleri.
Asitlerin Kuvvetli ve Zayıf Olduğunu Nasıl Anlarız?
Asitlerin sulu çözeltilerinde çözünen asit moleküllerinin asidin türüne göre bazen tamamı iyonlarına ayrılırken, bazen de bir kısmı iyonlarına ayrılır.
Farklı asitlerin suya H+ iyonu verme yatkınlıkları farklıdır, işte bu farklılık kuvvetli asit ve zayıf asit kavramlarının ortaya çıkmasına neden olur. Derişimleri aynı olan farklı asitlerin güçleri aynı değildir.
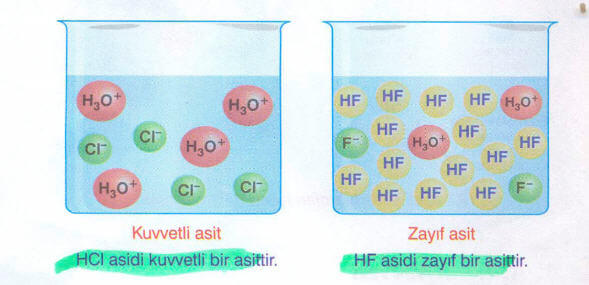
Çözeltilerde tamamen iyonlaşarak tüm protonlarını veren asitlere kuvvetli asit denir.
Çözeltilerde kısmen iyonlaşarak protonlarının bir kısmını veren asitlere de zayıf asit denir.
Kuvvetli bir asit çözeltisini suya ilave ettiğimiz zaman hidronyum iyonlarının derişiminde büyük bir artış olur. Örneğin, nitrik asit kuvvetli bir asittir. 1 litresinde 0,1 mol
çözünmüş olan çözeltide nitrik asit moleküllerinin % 92 si iyonlaşarak hidronyum ve nitrat iyonu oluştururlar.
Hidroklorik asit (HCl), hidrobromik asit (HBr), hidroiyodik (HI) asit ve sülfürik asit diğer kuvvetli asitlere örnektir.
NOT: Halojenlerin asitleri (F hariç) kuvvetli asittir. HF zayıf asittir. Diğerleri arasında HI > HBr > HCI kuvvet sırası vardır.
Bir zayıf asidin suya ilavesi hidronyum iyonlarının derişimini çok az artırır. Örneğin, zayıf bir asit olan asetik asidin 1 litresinde 0,1 mol asetik asit çözünmüş olan çözeltisinde asetik asit moleküllerinin ancak % 1,3 ü iyonlaşarak hidronyum ve asetat iyonlarını oluşturur.
Nitröz asit (), karbonik asit (
), borik asit (
) hidrojen florür asidi (HF) ve hidrojen siyanür asidi (HCN) zayıf asitlere örnektir.
| Bazı yaygın kullanılan kuvvetli asit ve zayıf asitler | |||
| Kuvvetli asitler | Zayıf asitler | ||
| Hidroklorik asit | HCl | Karbonik asit | |
| Sülfürik asit | Asetik asit | ||
| Nitrik asit | Fosforik asit | ||
| Kromik asit | Hidroflorik asit | HF | |