Antoine Lavoisier neyi buldu? Antoine Lavoisier’in yaptığı deneyler ve sonuçları, kimya bilimine katkıları nelerdir, hakkında bilgi.
A. L. LAVOISIER

Oksijen Varsayımının Kanıtı
Antoine Laurent Lavoisier 1743 yılında Paris’te doğdu. 1794’te yine aynı şehirde idam edilerek öldürüldü. Babası avukattı. Annesi o daha çocukken öldüğü için, teyzelerinden biri tarafından yetiştirildi. College Mazarin’de eğitim gördü, bakaloryasını 1763’te, lisansını 1764’te aldı. Lavoisier iki farklı görevi üstün başarıyla sürdürmeyi başardı. Tahsildar olarak devlet hizmetine girdi. Ama çok genç bir yaşta, büyük bir duyarlık ve canlılıkla bilimsel çalışmalara koyuldu. Tartışmalı geçen bir seçimden sonra, 1769’da Akademi üyeliği onaylandı ve 1778’de maaşlı üye oldu. Tahsildarlıkta da gösterdiği başarı, onu 1780’de Mültezim yaptı.
Eserinin niteliği kendi döneminde yaygınca biliniyordu. 1788’de “Royal Society”ye seçildi. Cavendish’in başlattığı ve Priestley’in geliştirdiği gaz kimyası çalışmalarını geniş bir alana yaymış ve bunları etkili bir şekilde birbirleriyle kıyaslamıştı. Bundan dolayı çalışmalarında İngilizlerin güçlü etkisini görmek mümkündür. 1771’de Marie-Anne Paulze ile evlendi. O da özellikle İngilizce alanında uzmanlaşmış iyi bir dilbilimciydi. Lavoisier eşinden büyük destek gördü. Bayan Lavoisier eşinin yazılarını İngilizceye çeviriyordu. İngiliz yazarların yapıtlarını da Fransızcaya çeviriyordu. Marie Anne Paulze, bir yandan Prusya toplarının namlu imalini denetlerken, öte yandan sıcaklık üzerine yaptığı gözlemlerle taranan sıra dışı bir bilim serüvencisi Kont Rumford ile evlenmekle hayat kurtarmıştı. Berzelius, Lavoisier’in ölümünden çok sonra Paris’e uğradığı bir sırada, bilimadamlarının doldurduğu bir salonda başkanlık ederken gördüğü Barones Rumford’un heybetli tavırlarım anlatır.
1789 Devriminden sonra, Lavoisier yeni kurulan devlet için çalıştı. Metrik sistemi yaymak için çalışan komisyonun üyesiydi. Ama eski düzenin bir aracı olmasının, hem de en haksız kolunun (vergi-toplayıcılar) bir uzantısı olmasının lekesi, üzerinden silinmedi. Diğer Mültezimler gibi tutuklanıp yargılandı. Davası “Devletin aydınlara ihtiyacı yoktur,” sözünden ötürü ünlenmiştir. Bu öğreti ister gerçekten savunulsun ister savunulmasın, Lavoisier kötü emellerinden dolayı suçlu bulundu ve 1794’te idam edildi.
Lavoisier’den önce yanma olgusu
Yanma olgusu, Lavoisier’in deneylerinden en az yüz yıl kadar önce, havanın bileşimi ve doğası ile ilgili çalışmaların çerçevesine oturtulmuştu. Esas adım 1673 yılında bir yerlerde John Mayow tarafından atılmıştı. Mayow (1643-1679) yanma ve solumanın neden olduğu hava seyrelmesi üzerine sistematik araştırmalar yapıyordu. Bunu havarim farklı zerreciklerden oluştuğu ve bunlardan bir türünün yanmada emildiği düşüncesiyle açıklamıştı. Mayow, Oxford’da 1647 yılında yayımlanan toplu yazılarında (Tractatus quinque me-dico-physici) yer alan De sal-nitro et spiritu-nitro-aereo başlıklı çalışmasında şu sonuca varıyor: “… hava, nitro-aerial dediğimiz, ateş için mutlak surette elzem olan birtakım zerrecikler içeriyor, bunlar alev çıkarken havadan çekilip bırakılıyor, böylece ateşi besleyecek durumdan çıkıyorlar.” Mayow ayrıca bu zerreciklerin havanın esnek gücünden de sorumlu olduğuna, bunların yokluğunda, havanın, hacmi azaltılarak, çok daha kolayca sıkıştırılabileceğine inanıyordu.
Ne yazık ki, Stephen Hales 1724 yılında bu çalışmaları yineleyerek ve kapsamım genişleterek işe koyulduğunda, esneklik konusuna eğildi ve gazların farklı bileşenleri ile ilgili kuramı bir tarafa bıraktı. Sınırlı miktarda hava içerisinde yanan burnun yarattığı etkiyi, azalan hacim miktarının, “mumun yanmasıyla esnekliği yok olan havanın miktarına eşit olması” varsayımı ile açıkladı. Bu düşünceyi hava solunumuna da uygulayarak, içindeki havadan birkaç nefes alınmış bir kesenin gevşek görüntüsünü ve “ciğerlerimin oldukça solgunlaştığım açıkça hissediyor” olmasını, “havanın canlandırıcı ruhunun tüketilmesi ve yitirilmesi yüzünden değil, havanın esnekliğinin hatırı sayılır bir bölümünün yok olmasından başka bir nedene atfedilemeyeceği” sonucuna vardı. Sonraki adım, Priestley’in havanın solunabilir kısmının başka araçlarla tamamlama yolları bulmasıydı.
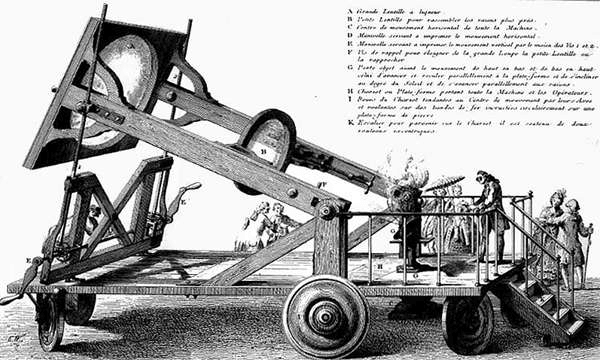
Kısmen Lavoisier’in gözetimi alfanda, Paris Bilimler Akademisi tarafından yaptırılan dev mercek.
Hava Üzerine Gözlemler’inde 1774’te yapılan bir deneyi anlatır:
“On iki inç çapında ve odak noktasına 20 inç uzaklıkta duran bir mercek koyduktan soma…, onun yardımıyla (yanan bir cam gibi), doğal ya da yapıntı çeşitli maddelerin ne tür hava ürettiklerini incelemeye koyuldum.” ‘Saf cıvalı kireç’e [cıvalı oksit] yüksek sıcaklık uygulayarak, suda kolayca çözünemeyen bir hava elde etti. “Ama beni, dile getiremeyeceğim kadar çok şaşırtan şey, bu hava içinde yanan mumun alev ve sıcaklığının” diğer havalarla kıyaslandığında, “muazzam olmasıydı.” Priestley, bu havayı solumaya çalıştı ve onda hoş ve canlandırıcı bir uyarıcı etkisi sezdi. “Kim bilir, belki de zamanla, bu saf hava lüks şeyler arasında rağbet görür. Şu ana dek sadece iki fare ve ben bunu koklama ayrıcalığına sahip olduk.”
Priestley buluşunu tamamen yanlış yorumladı. Mayow’un düşüncesini izlemedi. Bu yol onu, ürettiği “yapıntı hava”yı atmosferin solunabilir parçasıyla özdeşleştirmeye götürebilirdi. Hales gibi o da bir kuranım yandaşıydı. Her ikisinin doğru gördükleri kuramlar farklıydı belki ama, Priestley’inki, eldeki sonuçlan yanlış yorumlamasına yol açan bir kuramdı. Flojiston varsayımına inanıyordu. Bu kurama göre, yanma ve solunum süresince flojiston adı verilen “[havayı] solunum ve alevlendirme için elverişsiz hale gey ren, onu değiştiren” bir madde açığa çıkıyordu. Atmosferik havanın basit, temel bir madde olduğuna da inandığından buluşunu atmosferik havadan daha az flojiston içeren bir hava karışımı şeklinde yorumlaması gerekmişti. Bu hava, işte bu nedenle, yanmayı ve solunumu beslemek için, atmosferik havadan daha elverişliydi. Priestley şu sonuca vardı: “Havayı atmosferik havadan daha saf hale getirebiliriz, yani flojistondan arındırılmış bir hava… atmosferdeki havadan daha az flojiston içeren bir hava elde edebiliriz.”
Yanma Deneyi
Lavoisier’in çözümü basitti. Mayow’un düşüncesini, yani havanın, biri solunabilir ve yanmayı besleyen, öteki ‘zehirleyici’ ve yaşamı beslemeyen iki tür ‘hava’ ya da gaz karışımı olduğu düşüncesini yeniden ele adı. Priestley’in kuramını ve kimyasal olgulara ilişkin yorumlarını gözden geçirirken, “durumun farklı olduğuna dair hislerimi güçlendirdi, hem zaten ben, yanmadan sonra atmosferik hava kalıntısının zehirleyici kısım olduğuna, yanmanın dörtte üçünü oluşturduğuna, saf, solunabilir halini az ya da çok yitirdiğine dair bazı kanıtlar göstermiştim,” diyor. Bu görüşün deneysel testi, ki bu Priestley’in düşüncelerini de çürütecekti, solunabilir kısmı toz haline getirerek katılaştırmak, sonra onu birleşmiş olduğu maddeden çıkartmak, son olarak da gaz kalıntıya katmaktı. Eğer bu tekrar sıradan havayı üretiyorsa, sorun çözülmüş demekti. “Eğer, Dr. Priestley’in düşündüğü gibi, bu hava [kalıntı hava] kendisini yararsız kılan bir unsur tarafından kirletilseydi, yitirdiği kısmı ona geri kazandırmak yeterli olmazdı. Ama onu tekrar adi hava durumuna getirmek için, bu kirletici maddeyi de ondan ayırmak gerekir.”
Lavoisier, nefis bir ironiyle, Priestley’in saf hava hazırlamakta kullandığı yöntemin aynısını (yani cıva oksidi ısıtmak), havanın kayıp kısmım geri kazandırmak için kullandı. Ama buradaki numara şuydu: Cıva oksidin kendisi zaten cıvanın, alınan hava örneği içinde yavaş yanmasından oluşmuştu.

Lavoisier’nin ünlü deneyi için kullandığı aygıt. Bununla, yanma olayında oksijenin önemini göstermiştir.
Lavoisier deneyi şöyle anlatıyor:
“Uygun bir aygıtta, bunu çizim olmadan tasvir etmek zor, elli inç küp adi hava hapsedildi; buna çok saf qyadan dört ons koyup, on iki gün süreyle orda tutarak, hemen hemen kaynama derecesine yakın bir sıcaklık altında kireçleştirmeye [okside etmeye]koyuldum….
On ikinci gün ateşi söndürüp kabı soğuttuktan sonra, bunların içerdiği havanın … hacminin 1/6’sı kadar azaldığım gözledim: Aynı zamanda önemli bir miktar, aşağı yukarı kırk beş grain [0,325 gram], kireçleşmiş [oksitlenmiş] cıva oluştu, ••• bu durumda azalan hava … mumları söndürdü… Kısaca, tamamen zehirleyici duruma indirgenmiş oldu.”
Deneyin arkasındaki kilit uslamlama Lavoisier tarafından şöyle anlatılıyor: “Dr Priestley’in ve benim yaptığım de neylerde kanıtlanmıştır ki, kireçleşmiş cıva sadece bu metal ile onun ağırlığının yaklaşık 1/12’si kadar, deyim yerindeyse, adi havadan daha iyi ve solunuma daha uygun havanın karışımıdır: Söz konusu deneyde kanıtlandığı üzere cıvanın kireçleşmiş haliyle, havanın en iyi ve solunuma en uygun kısmım emdiği ve geriye zehirli ve teneffüs edilemez kısmının kaldığı görülüyor.” Şimdi yapılacak tüm iş emilen havayı yeniden kazanıp zehirli kalıntıya geri vermekti. Lavoisier’in yaptığı işte buydu. “Önceki deneyde oluşan kırk beş gram kireçleşmiş cıvayı ihtimamla topladım; ve bunu küçük bir cam imbiğe koydum. İmbiğin boğazı, ters çevrilerek suya kapatılmış bir cam fanusun alfandan geçebilecek şekilde kıvrılmıştı. Su miktarım hiç artırmamış, giderek azaltmıştım. Bu işlemle, kireçlenme sırasında emilen havamn hemen hemen tamamını yemden elde ettim… o işlemle bozulmuş hava ile yeniden birleştirildiği zaman, sonraki tamamen düzeldi, kireçleştirilmeden önceki durumuna, yani adi hava durumuna döndü.”
Mesele hallolmuştu neredeyse.
Atılacak bir iki adım daha kalmıştı. Oksidasyon ile solunumu bir araya getirmek ortaya yeni bir kuram çıkarıyordu. Bu amaçla Lavoisier, solunum işlemi üzerine biraz daha sıkı çalıştı. Lavoisier, “solunumla kirlenen havanın, 1/6 oranında kireçten elde edilene tamamıyla benzer, hava halinde asit içerdiğini” gösterdi. Solunum işleminde solunabilecek hava emiliyor, şimdiki deyimle, karbondioksit dışarı atılıyordu. Ama kimi tahminler biraz yoldan çıkmıştı, işte bir tanesi: “Bu metaller tamamen solunabilir hava ile güzel, kırmızı cüruflar oluşturuyor, …şimdi kanın renginin kırmızı olmasını, onun flojistondan arınmış hava ile birleşmesine bağlayamaz mıyız?” Çok daha yaygın terim “oksijen” yerine kullanılan bu tuhaf deyim, Priestley’in kendi buluşunu açıklamasını andırıyor. Eğer oksijen, ısıtma yoluyla cıva posasından ayrıştırılıyor ve cıva eski haline getirilebiliyorsa, flojiston kuramının karman çorman dünyasında, sonuç, oksijen açığa çıkmasıyla değil, havadan flojiston emilmesiyle doğrulanır. Öyleyse sonuç flojistondan arındırılmış hava olmalıdır.

Deney, hassas ölçülerle çalışıldığında, az bir çaba gerektiriyordu. Sadece yanma ilkesi ortaya konmuştu bu deneyle. Lavoisier, yanma üzerine niceliksel çalışmalara da girişti. Teçhizatın hantallığına karşın, şaşırtıcı doğruluktaydı bunlar. Kireçleşme süresince emiş için gerekli olan havayı, soğutma işleminden sonra imbiğe çekerek, bu havanın miktarım ölçtü. Emilen havanın ağırlığını tahmin edebilmişti. Bu deneylerde, farklı bir metal, kalay kullandı. Kireçleşmeden önce ve sonraki kalay miktarını ölçerek, cüruf ya da oksit oluşturmak için
kadar oksijen kullanıldığım hesaplayabildi. Modem standartlarla karşılaştırıldığında sonuçlar ikna edici görünmüyor. Ne var ki, kireçleşme sırasında havanın kaybettiği ama kalayın kazandığı ağırlığa ilişkin açıklaması, oksit kazanıldıkça havadaki oksijenden aynı miktarda kaybedildiği tezi ile uyumluydu.
Oksijen kimyası ile ilgili sonraki çalışmalar
Lavoisier’den sonra gazların kimyasında görülen gelişmeler, Mayow’un başlattığı, Cavendish ve Priestley’in yeniden düzenlediği ve Lavoisier’in zekâsında yukarıda anlatıldığı gibi filizlenen deneyler türünde radikal yeniliklerden çok, birbirini izleyen yenileştirmeler şeklindedir. Çok daha doğru niceliksel yöntemler 19. yüzyılda ortaya çıktı. Ancak bu yöntemlerle çeşitli kimyasal etkileşimlerde birleştirilen gazların ağırlıkları ile bu şekilde oluşturulan bileşiklerin ağırlığında görülen artışlar arasında kesin karşılaştırmalar yapmak olanaklı olabilirdi. Lavoisier inorganik maddeler kimyasında oksijenin yerini ciddi bir biçimde yanlış anlamıştı. Anlaşıldığı kadarıyla, Lavoisier eski düşüncelerden kendisini tamamen kurtaramamıştı. Ateş söz konusu olduğunda, flojiston ile ateş arasında özel bir etkileşim olduğu, sözgelimi ateşin havanın esnekliği üzerindeki etkisinde bunun belirginleştiği düşünülüyordu. Lavoisier oksijenin asitlerin birincil aktif bileşeni olduğunu düşünmüştü. Onun gazlar için kullandığı, “asit üretici” anlamına gelen “oksijen” terimini işte bu hataya borçluyuz. Ama bu, asitlerin gerçek mahiyetinin ortaya çıkarılmasından yaklaşık kırk yıl kadar önceydi.
Deneyi nasıl yorumlamalıyız? Lavoisier’in oksijeni keşfettiğini söylemek tamamen doğru olmayacaktır. Hem sonra, Mayow da, Priestley de bir malzemeyi belirlemişlerdi. Ama Mayow spiritus nitro-aereus’u keşfetti, Priestley ise, flojistondan arındırılmış havayı… Olgusal bir meseleyle uğraşmıyoruz, ama bilinen olguları bir düzene koymakta kullanılan rakip kavramsallaştırmaların ne derece uygun olduğunu sınıyoruz; burada “madde”nin varoluşu söz konusu edilmemektedir.