Oksijen elementinin özellikleri, atom numarası, keşfedilmesi, bileşikleri, periyodik cetveldeki yeri, kullanım alanları, Oksijen elementi ile ilgili bilgi.
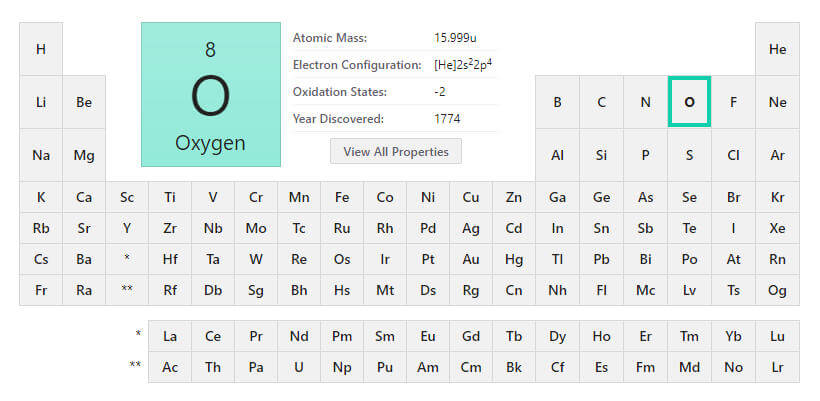
Oksijen
Oksijen gazı atmosferin yaklaşık beşte birini kaplar. Mars atmosferinde yalnızca % 0.15 oranında oksijen bulunur. Oksijen, karbon-azot döngüsünde önemli bir rol oynar. İnsan vücudunun yaklaşık üçte ikisi, suyun onda dokuzu oksijendir. Oksijen gazı renksiz, kokusuz ve tatsızdır. Oksijenin sıvı ve katı hali soluk mavi renktedir.
Sembolü: O
Atom Numarası: 8
Atom Ağırlığı: 15.9994(3) g·mol−1
Elektron Sayısı: 8
Elemet serisi: Halojen
Periyodik Tablodaki Yeri: Grup 16A
Maddenin Hali: Gaz
Görünümü: Renksiz
Oksijenin Keşfi ve Tarihçesi
Oksijen ilk olarak, 1772 yılında Carl Wilhelm Scheele tarafından keşfedilmiştir. Ancak Joseph Priestley de iki yıl sonra oksijeni güherçilerin kavrulması ve daha sonra kırmızı cıva oksidin ısıtılmasıyla keşfetmiş ve bunun haberini Scheele’den önce yaydığından, pek çok kimse tarafından ilk onun keşfettiği düşünülür.
1775’ten sonra Lavoisier oksijenin temel özelliklerini açıklayarak suda ve havada bulunduğunu, yanma ve solunumdaki işlevini gösterdi. Asitlerin bileşiminde kesinlikle bu elementin bulunduğuna ve asitlik nedenini ortaya çıkaracağına inanarak oksijenle ilgili bir dizi deneyler gerçekleştirdi ve bu elemente asit üreten anlamına gelen oksijen adını verdi. Oksijen ismi Yunanca oxus (asit) ve gennan (oluşturmak) sözcüklerinden gelir.
Yeryüzünde en çok bulunan elementtir. Toplam olarak yeryüzündeki suların yaklaşık % 89′ unu, kayalarınsa yaklaşık olarak % 47′ sini, atmosfer kütlesinin % 23 unü ve hacminin % 21’ini oluşturur. Bu yüzden olağan koşullar altında gaz halinde bulunan oksijen, sıvılaştırılmış havadan basamaklı damıtmayla elde edilebilir. İnsan vücudunun üçte ikisi, suyun ise onda dokuzu oksijendir. Sıvılaştırılması güç bir gazdır. Ancak sıvılaştırılmış oksijen mavi renktedir. Su az çözünür buna karşın ergimiş gümüşte çok miktarda eriyerek gümüşün katılaşması sırasında açığa çıkar. Oksijenin morötesi ışınların yada elektrik boşalmalarının etkisinde kalması sonucunda çok etkin bir oksijen allotropu olan Ozon oluşur.
Oksijen tüm canlıların solunumu ve uygulamada tüm yanma olaylarının gerçekleşebilmesi için gerekli temel maddedir. Oksijen havadan ve elektroliz yoluyla sudan elde edilebilir. Dünyada kullanılan oksijenin % 99’u havadan, % l’i ise sudan elde edilir. Dünya saf oksijen üretimi yaklaşık olarak günde 50 milyon metreküpü bulur, bunun yarısına yakın bölümü çelik üretme fırınlarında ve değiştirgeçlerdeki arıtma işlemi sırasında kullanılır. Bundan başka amonyak, metanol, etilenoksil gibi gazların sentezine sıvı hidrojenle birlikte, füze motorlarında propergol olarakta kullanılır.

Kullanım Alanları:
Oksijen yanmayı mümkün kılan gazdır. Bir nesne yanarken oksijeni kullanır, ısı ve ışığı serbest bırakır. Bu özelliğinden dolayı oksijenin birçok kullanım alanı vardır. Ama, aynı zamanda saf oksijen çok tehlikelidir. Saf oksijene, bir alev ya da kıvılcım dokunursa, çok büyük bir yanma ve hasara neden olabilir.
Yanma özelliği, birçok şekilde kullanılabilir. Örneğin, oksijen asetilen ile karıştırıldığı zaman, çok sıcak bir alev oluşturabilirsiniz. Oksijen kaynağı metalleri birleştirmede kullanılan bir kaynak çeşididir. Ayrıca, oksijen, roket ve jetleri için güçlü yakıtlar oluşturmak için kullanılır.
Oksijenin Kullanım Alanları Daha Fazlası

Oksijenin Elde Edilmesi:
Ozon (O3), oksijenin bir Allotropudur. Dünyanın yüzeyine ulaşan güneşin zararlı ultraviyole ışınlarını önlemeyen bir tabaka oluşturduğundan hayati önem taşır. Aerosollerin atmosferdeki ozon tabakası üzerinde zararlı etkileri vardır. Kutup bölgeleri üzerindeki ozon tabakasındaki büyük deliklerin boyutları bu yıl artmaktadır. Paradoksal olarak, ozon zehirlidir! Sulandırılmamış ozon mavimsi renklidir. Sıvı ozon mavimsi siyah ve katı ozon mor-siyahtır.
Oksijen çok reaktif bir gazdır ve bir çok elementin oksitlerini oluşturur. Tüm bitkilerin ve hayvanların solunumları için gereklidir.
Bileşikleri
Oldukça aktif bir bileşik olan ozon (O3), elektriksel bir deşarj veya ultraviyole ışığın oksijen üzerindeki etkisiyle oluşur.
Ozonun atmosferdeki varlığı (sıradan basınçlar ve sıcaklıklar altında 3 mm kalınlığında bir katmanın eşdeğeri olan), güneşin zararlı ultraviyole ışınlarının dünya yüzeyine ulaşmasını önlemeye yardımcı olur. Atmosferdeki kirleticilerin bu ozon tabakası üzerinde zararlı bir etkisi olabilir. Ozon zehirlidir ve maruziyet 0,2 mg / m # ‘ı (8 saatlik zaman ağırlıklı ortalama – 40 saatlik çalışma haftası) geçmemelidir. Seyreltilmemiş ozon mavimsi bir renge sahiptir. Sıvı ozon mavimsi siyah ve katı ozon menekşe-siyahtır.
24 yorum
müthiş……………………………………basarılı
İyimiş
çok güzelllll
performansa işe yaradı
çok iyiymiş ya :):):) çok sağolun
cok guzel
super
acayip güzel site işime çok yaradı
ezberledim yaaaaaaa cok işime yaradı
Süper 😉 🙂 😀
çok yazı var ya hepsini yazamam
çok güzel yüz alırsam size çok dua etcem bi imam hatipli olarak 😀
çookk güzeelll 🙂
harikaymış teşekkür ederim
maşallah kimse beğenmemezlik yapmamamış
çook tesekkur ettim…. muhteşem bir teorim var eğer doruluğunu ispat edersem evrenn hakkında ki bilgilerin neredeyse tamamını dış uzayı arastırmadan öğrnebileceğizz..!
cok güzel
çok güzel
harika
çok güzel bütün element ödevlerimi buradan yaptım
allahınıza kurban
mühteşemmm
Cok tesekkur ederim
Byıldım çok güzel