Ametaller hangileridir? Ametallerin özellikleri, periyodik cetveldeki yerleri, elektron dizilimleri, önemli metaller hakkında bilgi.
AMETALLER
Yaşamımızı sürdürebilmek için olmazsa olmazlardan oksijen, soluduğumuz havadaki azot ve hidrojen, tarımda zirai ilaç olarak kullanılan kükürt, kibritlerde kullanılan fosfor, su arıtımında kullanılan klor ametallerden sadece bazılarıdır.
Önemli Ametaller
Hidrojen: H
Azot: N
Oksijen: O
Flor: F
Fosfor: P
Kükürt: S
Klor: Cl
İyot: I
Ametallerin özellikleri
***Ametaller kırılgan bir yapıya sahip olduğundan işlenmeleri zordur. Dolayısıyla büyük çoğunluğu tel ve levha haline getirilemezler.
***Ametaller elektrik ve ısıyı ya iletmezler ya da çok az iletirler. O yüzden daha çok yalıtım malzemesi olarak kullanılırlar.
***Oda sıcaklığında yani 25° C sıcaklıkta bazı ametaller katı halde (kükürt, fosfor, iyot gibi); bazı ametaller sıvı halde (brom gibi) ve bazı ametaller gaz halde (hidrojen, oksijen, azot gibi) olabilirler. Ametaller oda sıcaklığında katı, sıvı veya gaz halinde olabilirler.
***Ametallerden katı olanların yüzeyleri mattır.
***Son katmanında 5, 6 veya 7 elektron olan elementler genelde ametaldir. Son katmanında 1 elektron olan hidrojen, 4 elektron olan karbon ametal özelliği gösteren istisna elementlerdir.

***Ametaller, düşük yoğunluklu, erime ve kaynama noktaları düşük maddelerdir.
***Daha önce elektron diziliminin son katmanında bulunan elektron sayısının elementin periyodik cetveldeki grubunu verdiğini öğrenmiştik. Ayrıca ametallerin son katmanlarında genelde 5, 6 veya 7 elektron olduğunu da öğrendik. O halde periyodik cetvelin 5A, 6A ve 7A gruplarında genelde ametaller bulunur.
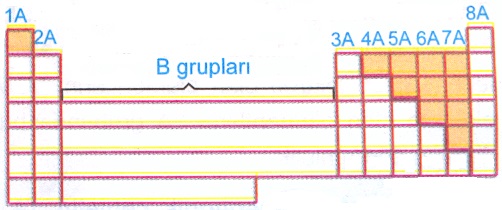
***Yukarıdaki periyodik tabloda ametallerin bulunduğu bölgeler taranmıştır. Ancak biz sadece ilk 20 elementle ilgileneceğimiz için 5A, 6A ve 7A grubunda bulunan elementleri ametal olarak kabul edeceğiz.
***Son katmanında 5, 6 veya 7 elektron olan elementlerin elektron alıp son katmanlarındaki elektron sayısını sekize tamamladığını; yani oktete ulaşarak kararlı hale geçer. Aynı zamanda elektron alan atomun (-) yüklü iyon oluşturduğunu da öğrenmiştik. Bu bilgiye göre;
• 5A grubundaki elementlerin son katmanlarında 5 elektron bulunur. Elektron sayısını sekize tamamlamak için 3 elektron alırlar. Bu durumda -3 yüklü iyon oluştururlar.
• 6A grubundaki elementlerin son katmanlarında 6 elektron bulunur. Bunu 8 e tamamlamak için 2 elektron alırlar. Bu durumda -2 yüklü iyon oluştururlar.
• 7A grubundaki elementlerin son katmanlarında 7 elektron bulunur. Bunu 8 e tamamlamak için 1 elektron alırlar. Bu durumda -1 yüklü iyon oluştururlar.