Aromatik bileşikler nelerdir? Aromatik bileşiklerin yapısı, kullanım alanları ve özellikleri nelerdir? Aromatik bileşikler hakkında bilgi.
Aromatik Bileşikler Nelerdir? Özellikleri
Aromatik bileşikler, organik kimyasal bileşiklerin, halkalı molekül yapıları ve oldukça değişik özellikleriyle alifatik bileşiklerden ayrılan çok geniş bir sınıfıdır. “Kokulu” anlamındaki aromatik terimi ilk kez 1860’a doğru, kömür katranından ayrılan ve keskin kokularıyla öbür hidrokarbonlardan ayırt edilen bir grup hidrokarbon için kullanılmıştır. Gerçekten de, örneğin karanfil, tarçın, anason, vanilya gibi baharatların uçucu yağlarından elde edilebilen aromatik bileşiklerin hepsinin kendine özgü, hoş bir kokusu vardır. 1861’de Avusturyalı kimyacı Joseph Loschmidt, pek çok aromatik bileşiğin formülünün benzen molekülündeki bir ya da birkaç hidrojenin yerine başka atom ya da atom gruplarının geçmesiyle türetilebileceğini gözlemledi. Daha sonra, aromatik terimi bu ilk anlamını yitirdi ve kimyacılar için, yapısal olarak benzenden türemiş herhangi bir bileşik anlamını kazandı.
Bugün kimyada aromatiklik kavramı, özellikle, bu tür bileşiklerin elektron yapılarından ileri gelen düşük tepkime eğilimini belirtir. Gerçekten de, iki ayrı türden ortaklaşım bağıyla (kovalans bağı) birbirine bağlanmış karbon atomlarının oluşturduğu bir ya da daha fazla sayıda düzlemsel halkadan oluşan aromatik bileşikler, doymamış yapıda olmalarına karşın, kolaylıkla tepkimeye girmezler; örneğin kolayca yükseltgenmez ve katılma tepkimelerinden çok ornatma tepkimelerine yönelirler. 1930’larda aromatiklik kavramının kapsamı büyük ölçüde genişletilmiştir. Giderek, benzen türevi aromatik bileşiklerin yanı sıra, benzen dışı aromatik bileşikler de tanımlanmıştır.
Aromatik bileşiklerin çoğu, molekülünde altı karbon atomlu bir halka bulunan benzenle akrabadır.
Çok kalabalık ve sanayi açısından çok daha önemli olan bu sınıfın dışında kalan aromatik bileşiklerde ise. Bir ya da birkaç karbon atomunun yerini başka elementlerin (özellikle azot) atomları alır. Aromatik halkadaki her atom, iki yanındaki iki atomla birer elektron çiftini bölüşür (ortaklaşım bağı); bu elektron çiftlerinden her biri, birbirine komşu iki karbon atomu arasındaki bölgede ve iki karbon çekirdeği arasından çizilecek bir eksene göre bakışımlı olan bir yörünge üstünde yerleşerek bir (sigma)bağı oluşturur.
Ayrıca, o bağları gibi doğrudan doğruya iki komşu çekirdek arasında yer almaz. İki karbon ile bu karbonlara bağlı atomların oluşturduğu molekül düzleminin hemen altında ve hemen üstündeki bir yörüngeye yerleşmiş elektron çiftlerinin oluşturduğu Π(pi) bağları bulunur. Bu Π bağları (ya da ti elektronları) herhangi bir atom çiftine değil, halkanın tümüne aittir. Aromatik bileşiklerin temel özelliği de, halkadaki atomların sayısından ya da türünden çok, n -bağ sistemindeki elektronların sayısına bağlıdır. Genellikle altı elektron içeren bu bağ sisteminde, n =1,2,3, vb olmak üzere 4n +2 ifadesiyle belirtilebilecek sayıda elektron bulunabilir.
Benzen türevi aromatik bileşikler.
Benzenden türeyen aromatik hidrokarbonlar sınıfı genellikle arenler adıyla bilinir. Organik kimyanın bu dalı oldukça erken bir tarihte, genel olarak alifatik kimyanın doğuşundan ve düzenli bir adlandırma sisteminin kuruluşundan önce gelişti. Bu yüzden aromatik bileşikler alifatik bileşiklerde olduğu gibi bilimsel adlandırmayla değil, daha çok cins adlarıyla anılır. Örneğin,
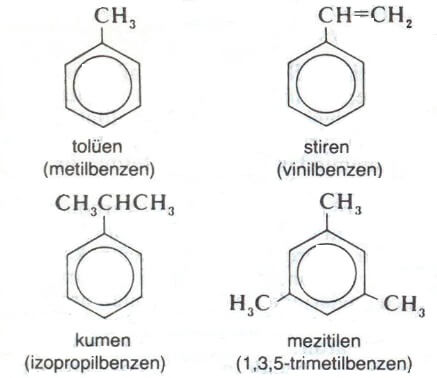
İki ornatmalı türevlerin, ksilende(dimetil-benzen) olduğu gibi, bir benzen halkası üzerinde orto (o) , meta (m) ve para (p) konumlarına yerleşmiş üç ayn izomeri olabilir:

Bazen, bu bileşiklerin yapısına katılan fenil ve benzil grubu gibi ornatma gruplarına ya da yan zincirlere aromatik grup, benzen halkasına ise aromatik çekirdek adı verilir.
Bir aromatik hidrokarbonda en az altı karbon atomu bulunur. O yüzden bu maddelerden hiçbirinin molekülü oda sıcaklığında gaz halinde bulunabilecek kadar küçük değildir. Benzen; p-ksilen, duren ve heksametil benzen gibi bakışımlı yapıdaki aromatik bileşiklerin erime noktası, daha az bakışımlı yapıdaki benzer bileşiklerden daha yüksektir. Düşük sıcaklıkların ölçülmesinde kullanılan termometrelerde, -39°C’de donan cıvanın yerine, donma noktası düşük (—95°C), genleşme katsayısı yüksek olan tolüen tercih edilir. Aromatik hidrokarbonlar, boya, vernik, yapay emaye gibi pek çok madde için alkanlardan daha iyi bir çözücüdür. Ancak, aromatik çözücülerle çalışıldığında. ortamın yeterince havalandırılması gerekir; çünkü çok küçük yoğunluklarda bile zehirli olan bu maddeler, özellikle benzen buharları uzun süre solunduğunda alyuvarların yıkımına yol açabilir.
Aromatik bileşikler kimyası 19. yüzyılın ilk yarısında, özellikle Almanya ve İngiltere’de kömürden aydınlatma gazı ve kok üretiminin başlamasından sonra gelişmiştir. Bu işlemin yan ürünü olan kömür katranı, ağırlığının yaklaşık yüzde 25’i oranında aromatik hidrokarbonlar içerir. Oysa günümüzde, aromatik hidrokarbon üretiminin en az yüzde 80’i petrol kökenlidir. Bu hidrokarbonlardan bazılarının ham petrolün bileşiminde bulunmasına ve doğrudan elde edilebilmesine karşılık, büyük bir bölümü alkanlardan, katalizör eşliğinde hidrojen giderme yöntemiyle (reforming) üretilir.
Yapısında birden fazla sayıda benzen halkası bulunan çok halkalı aromatik bileşikler, özellikle birçok aromatik halkanın iki ya da daha çok karbon atomunu ortaklaşa bölüştüğü naftalin, antrasen, fenantren gibi kaynaşmış ya da yoğunlaşmış halkalı aromatik bileşikler sanayi açısından daha önemlidir.
Benzen dışı aromatik bileşikler.
Benzenin ve benzer yapıdaki bileşiklerin aromatik özelliklerinin, altı karbonlu halkadaki eşlenik çift bağlardan kaynaklandığı anlaşıldı. Sonrasında, organik kimyacılar doğal olarak, eşlenik çift bağları olan daha büyük ve daha küçük halkalı bileşikleri bireşim yoluyla üretme olanaklarını araştırmaya başladılar. İlk amaç olan formülündeki siklobütadien ve türevlerini bireşim yoluyla elde etme girişimleri başarısızlıkla sonuçlandı. 1915’te Alman kimyacı Richard Willstâtter, aromatik bileşiklerden farklı olarak ornatma tepkimeleri yerine katılma tepkimelerine eğilimi olan, özetle aromatik bileşiklerden çok polienlere benzeyen siklooktatetraeni (
) bireşimle üretebildi. Sonraki yıllarda ise, azulen, siklodekapentaen gibi bütünüyle aromatik özellikler taşıyan benzen dışı hidrokarbonların bireşimi gerçekleştirildi. Halkalı, düzlemsel ve eşlenik sistemlerin aromatik olabilmesi için, neden 4nΠ(ör. 4,8,12,…) ya da herhangi bir sayıda elektron değil de ancak ve ancak 4n +2 Π sayıda (ör. 2,6,10,14,…) elektron içermesi gerektiğini kuramsal olarak açıklayan da Alman kimyacı Erich Hückel oldu.